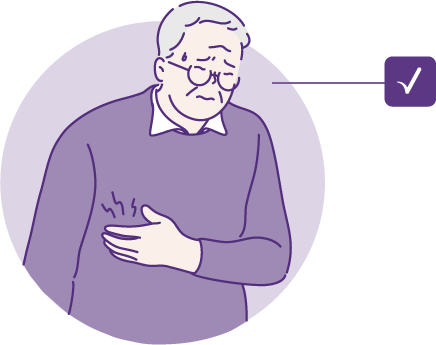
나이가 들수록 면역력이 저하되어 감염에 대응하는 능력이나 백신 접종 후 보호 면역 반응을 활성화하는 능력이 감소하게 됩니다.2
 아렉스비
아렉스비 
 아렉스비 접종 가능한
아렉스비 접종 가능한 아렉스비는 50-59세 고위험군과 60세 이상 성인에서 호흡기세포융합바이러스(RSV; Respiratory Synsytial Virus)에 의한 하기도 질환 예방에 적응증을 가진 RSV 백신입니다.
아렉스비 백신은 항원 특이적 세포성 면역 반응 및 RSV-A 및 RSV-B에 대한 중화 항체 반응을 촉진시켜 RSV 관련 하기도 질환 면역에 기여합니다.

나이가 들수록 면역력이 저하되어 감염에 대응하는 능력이나 백신 접종 후 보호 면역 반응을 활성화하는 능력이 감소하게 됩니다.2
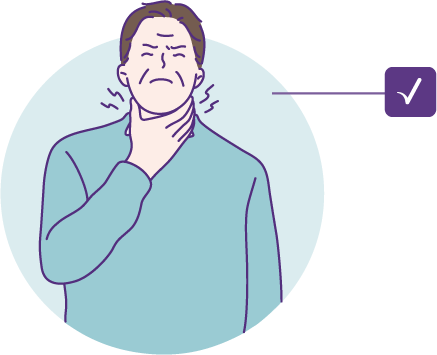
RSV와 연관된 하기도 질환(lower respiratory tract disease, LRTD) 발생의 위험성은 연령과 기저질환의 존재에 따라 증가합니다.
50-59세 이상 고위험군과
60세 이상 성인에서
호흡기세포융합바이러스
(RSV)에 의한 하기도 질환의
예방을 위해 투여합니다.


1회 0.5 mL를
근육주사로만 투여하며,
삼각근에 투여하는 것을
권장합니다.


불활화 계절성 인플루엔자
백신과 병용 투여할 수
있습니다.

아렉스비는 60세 이상 성인에서 82.6%의 RSV-하기도 질환 예방 효과를,
COPD, 천식 및 만성 호흡기/폐 질환 및 만성 심부전 등의 동반질환*을 1가지 이상 나타내는 60세 이상 성인에서는 94.6%의 예방
효과를 보였습니다.3

82.6%
(96.95% Cl: 57.9 - 94.1)
1차 평가변수
아렉스비 (7 cases out of 12,466),
위약 (40 cases out of 12,494)

94.6%a
(95% Cl: 65.9 - 99.9)
2차 평가변수
아렉스비 (1 cases out of 4,937),
위약 (18 cases out of 4,861)
동반질환은 COPD, 천식, 만성호흡기/폐 질환, 만성 심부전, 제1형 및 제2형 당뇨병, 진행성 간 또는 신장 질환
a 다중성(multiplicity)이 보정되지 않은 2차 평가변수; b 동반질환은 COPD, 천식, 만성 호흡기/폐 질환, 만성 심부전, 제1형 및 제2형 당뇨병, 진행성 간 또는 신장 질환입니다.3
CI: Confidence Interval; COPD: Chronic Obstructive Pulmonary Disease; LRTD: Lower Respiratory Tract Disease; RSV: Respiratory Syncytial Virus
[Study design] This is an ongoing, international, placebo-controlled, phase 3 trial, we randomly assigned, in a 1:1 ratio, adults 60 years of age or older to receive a single dose of an AS01E-adjuvanted RSV prefusion F protein–based candidate vaccine (RSVPreF3 OA) or placebo before the RSV season. The primary objective was to show vaccine efficacy of one dose of the RSVPreF3 OA vaccine against RSV-related lower respiratory tract disease, confirmed by reverse-transcriptase polymerase chain reaction (RT-PCR), during one RSV season. Efficacy against severe RSV-related lower respiratory tract disease and RSV-related acute respiratory infection was assessed.
아렉스비 구성 성분에 과민반응이 있는 경우에는 접종을 피해 주세요.
급성 중증 열성 질환을 앓고 있는 환자는 아렉스비 백신의 접종을 연기해 주세요.
혈소판 감소증이나 다른 혈액응고장애가 있는 환자는 근육주사 시 출혈이 일어날 수 있으므로 투여 시 주의해 주세요.
다른 백신과 마찬가지로, 이 백신이 모든 접종자에게 보호 면역 반응이 나타나지 않을 수 있습니다.
면역 억제 요법 중인 환자 또는 면역 결핍 환자는 아렉스비 백신에 대해 감소된 면역 반응을 나타낼 수도 있습니다.
안전성 프로파일은 60세 이상의 성인에 대해서 실시한 제3상 위약 대조 임상시험 결과,
매우 흔하게(≥1/10) 보고된
약물이상반응은 주사 부위 통증(60.9%), 피로(33.6%), 근육통(28.9%), 두통(27.2%) 및 관절통(18.1%)이었습니다.
보다 자세한 사항은 아렉스비 제품설명서를 참고해 주세요.
Tracy J. Ruckwardt. The road to approved vaccines for respiratory syncytial virus. npj Vaccines 2023 8:138.
Crooke SN et al. Immunosenescence and human vaccine immune responses. Immunity & Ageing. 2019;16:25.
Papi A, et al. Severe Morbidity and Short- and Mid- to Long-term Mortality in Older Adults Hospitalized with Respiratory Syncytial Virus Infection. NEJM 2023;388(7):595-608.
사용상의 주의사항 1. 다음 환자에는 투여하지 말 것 이 백신의 구성 성분에 과민반응이 있는 자 2. 다음 환자에게는 신중히 투여할 것 1) 급성 중증 열성 질환을 앓고 있는 자(급성 중증 열성질환이 있는 경우, 이 백신의 접종을 연기해야 한다) 2) 혈소판 감소증이나 다른 혈액응고장애가 있는 자(근육주사 시 출혈이 일어날 수 있으므로 주의하여 투여해야 한다.) 3. 이상사례 1) 유효성 임상시험(RSA-OA=ADJ-006) 안전성 프로파일은 60세 이상의 성인에 대해서 실시한 제3상 위약 대조 임상시험에서 이 백신을 1회 투여 받은 12,467명과 위약을 투여 받은 12,499명을 기반으로 한다. 이 임상시험에서 매우 흔하게(≥1/10) 보고된 약물이상반응은 주사 부위 통증(60.9%), 피로(33.6%), 근육통(28.9%), 두통(27.2%) 및 관절통(18.1%)이었다. 중대한 이상사례(SAEs, Serious Adverse Events) 임상시험에서 백신 접종 후 6개월 이내에 발생한 중대한 이상사례는 이 백신(4.2%) 또는 위약(4.0%)을 투여 받은 시험대상자들에게서 유사한 비율로 보고되었다. 백신 접종 후 6개월 이내에 이 백신을 투여 받은 시험대상자 13명과 위약을 투여 받은 시험대상자 15명에서 심방세동이 보고되었다. 4. 일반적 주의 1) 다른 백신과 마찬가지로, 백신 접종 후 아나필락시스 반응이 일어날 경우에 대비하여 적절한 의학적 치료 및 감독이 항상 준비되어 있어야 한다. 2) 다른 백신과 마찬가지로, 이 백신이 모든 접종자에게 보호 면역 반응이 나타나는 것은 아니다. 3) 주사침 투여로 인한 심리적 반응으로서 백신 접종 후 나 접종 전에 실신이 나타날 수 있다. 실신으로 인한 상해를 방지하기 위한 절차가 준비되어 있는 것이 중요하다. 4) 이 백신을 혈관내 또는 피내로 투여하지 않는다. 이 백신의 피하투여와 관련된 자료는 없다. 5) 면역저하자에 대한 이 백신의 안정성 및 면역원성 자료는 없다. 면역 억제 요법을 받고 있는 환자나 면역 결핍 환자는 이 백신에 대해 감소된 면역 반응을 나타낼 수도 있다. 5. 상호작용 이 백신은 비-면역증강 불활화 계절성 인플루엔자 백신과 병용 투여할 수 있다. 다른 백신과 병용 투여 시 서로 다른 주사 부위에 투여해야 한다. 6. 임부 및 수유부에 대한 투여 1) 임부 임부에서 이 백신을 사용한 자료는 없다. 임신 중 이 백신의 사용은 권장되지 않는다. 2) 수유 이 백신이 사람 또는 동물의 모유로 분비되는지 여부에 대한 자료는 없다. 수유 중 이 백신의 사용은 권장되지 않는다. 3) 수태능 사람의 수태능에 대한 이 백신의 영향과 관련된 자료는 없다. 동물시험에서 암컷의 수태능 면에서 직접적 또는 간접적인 유해한 영향이 나타나지 않았다. 7. 소아에 대한 투여 소아에서의 안전성 및 유효성은 확립되지 않았으며 관련 자료가 없다.